|
Neuer möglicher Mechanismus für die Entstehung von Leben
Redaktion
/ idw / Pressemitteilung des Max-Planck-Institut für Dynamik und
Selbstorganisation
astronews.com
17. August 2023
Moleküle können aktive Cluster bilden, die
Stoffwechselprozesse katalysieren, indem sie selbsterzeugten
Konzentrationsgradienten folgen. Dies ist das Ergebnis einer jetzt vorgestellten Studie.
Das Modell beschreibt die Selbstorganisation von Molekülen, die an
Stoffwechselwegen beteiligt sind und fügt so der Theorie über den Ursprung des
Lebens einen möglichen neuen Mechanismus hinzu.
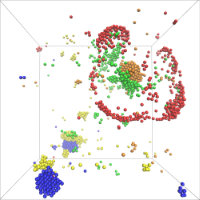
Ein neues Modell beschreibt die
Selbstorganisation von katalytischen Molekülen, die an
Stoffwechselzyklen beteiligt sind. Verschiedene Arten von
Katalysatoren (dargestellt durch unterschiedliche Farben)
bilden Cluster und können sich gegenseitig verfolgen.
Bild:
Vika Novak MPI-DS / LMP [Großansicht] |
Ein mögliches
Szenario für den Ursprung des Lebens ist die spontane Organisation von
interagierenden Molekülen zu zellartigen Tröpfchen. Diese bilden in der Folge
die ersten selbstreplizierenden Stoffwechselzyklen, welche in der Biologie weit
verbreitet und in allen Organismen zu finden sind. Diesem Szenario nach müssten
sich die ersten Biomoleküle dabei durch langsame, allerdings überwiegend
ineffiziente Prozesse zusammenschließen. Eine solch langsame Clusterbildung
scheint unvereinbar mit der Geschwindigkeit, mit der das Leben entstanden ist.
Wissenschaftler der Abteilung Physik der lebenden Materie des des
Max-Planck-Instituts für Dynamik und Selbstorganisation (MPI-DS) haben nun
ein alternatives Modell vorgeschlagen, das eine solche Clusterbildung von
katalytisch aktiven Molekülen und damit das schnelle Einsetzen der für die
Entstehung von Leben erforderlichen chemischen Reaktionen erklärt. "Dazu haben
wir verschiedene Moleküle in einem einfachen Stoffwechselzyklus betrachtet, bei
dem jedes Molekül oder Partikel eine Chemikalie produziert, die von dem nächsten
verwendet wird", berichtet Vincent Ouazan-Reboul, Erstautor der Studie. "Die
einzigen Bestandteile des Modells sind dabei die katalytische Aktivität der
Moleküle, ihre Fähigkeit einem selbsterzeugten Konzentrationsgradienten der
Chemikalien zu folgen, sowie die Information über die Reihenfolge der Moleküle
im Zyklus."
Unter diesen Voraussetzungen zeigt das Modell die Bildung von katalytischen
Clustern, die verschiedene Molekülarten enthalten. Das Wachstum von Clustern
erfolgt zudem exponentiell: Die Moleküle können sich also sehr schnell und in
großer Zahl zu dynamischen Strukturen zusammensetzen. Darüber hinaus spielt die
Anzahl der Molekülspezies, die am Stoffwechselzyklus teilnehmen, eine
Schlüsselrolle für die Struktur der gebildeten Cluster. "Unser Modell führt zu einer
Fülle komplexer Szenarien für die Selbstorganisation und macht spezifische
Vorhersagen über funktionelle Vorteile, die sich bei einer ungeraden oder
geraden Anzahl von beteiligten Spezies ergeben. Bemerkenswert ist, dass die
nicht-reziproken Interaktionen als notwendiger Bestandteil in unserem
vorgeschlagenen Szenario in allen Stoffwechselzyklen zu beobachten sind."
In
einer anderen Studie fanden die Autoren heraus, dass Selbstanziehung von
Molekülen für die Clusterbildung in einem kleinen Stoffwechselnetzwerk nicht
erforderlich ist. Stattdessen können Netzwerkeffekte dazu führen, dass sich
sogar eigentlich abstoßende Molekülspezies zu Gruppen zusammenschließen. Damit
zeigen die Forscher neue Bedingungen auf, unter denen komplexe Wechselwirkungen
selbstorganisierte Strukturen schaffen können. Insgesamt fügen die neuen
Erkenntnisse der Studien der Theorie zur Entstehung des Lebens aus einfachen
Molekülen einen weiteren Mechanismus hinzu. Sie decken auf, wie an
Stoffwechselnetzwerken beteiligte Moleküle selbstständig komplexe Strukturen
bilden können.
Über die Ergebnisse berichtet das Team in einem Fachartikel, der in der
Zeitschrift Nature Communications erschienen
ist.
|

